Vektor-Vakzine Ad26.COV2.S (Janssen / Johnson & Johnson)
Die nur einmalig zu verabreichende Vektor-Vakzine Ad26.COV2.S (Janssen / Johnson & Johnson) stellt den vierten in der Europäischen Union verfügbaren Impfstoff gegen COVID-19 dar.
Die Europäische Arzneimittelagentur (EMA) und auch das Paul-Ehrlich-Institut haben der humanen Adenovirus Type 26 (Ad26) Vektor-Vakzine Ad26.COV2.S des Herstellers Janssen / Johnson & Johnson die bedingte Zulassung erteilt.
Zwischenzeitlich hatte die US-amerikanische FDA die Impfungen wegen einiger Fälle einer VITT / VIPIT (The New England Journal of Medicine) vorübergehend gestoppt, nach eingehender Nutzen-Risiko-Bewertung aber wieder freigegeben. Wir hatten über diese sehr seltenen Ereignisse im Zusammenhang mit dem AstraZeneca-Impfstoff Vaxzevria berichtet.
Die internationalen Phase-I / II-Studien zu Ad26.COV2.S zeigten eine starke Antikörperantwort bereits nach einmaliger Verabreichung einer Dosis von 5 x 1010 Viruspartikeln, was momentan ein Alleinstellungsmerkmal unter den bisher zugelassenen Impfstoffen darstellt.
Im New England Journal of Medicine wurden nun die Ergebnisse der placebokontrollierten Phase-III-Studie (ENSEMBLE, The New England Journal of Medicine) veröffentlicht, welche zwischen September 2020 und Januar 2021 in den USA, Lateinamerika und Südafrika durchgeführt wurde.
Insgesamt wurden 21.895 Teilnehmende per Zufall der Ad26.COV2.S- und 21.888 der Placebo-Gruppe zugeteilt. Die Inzidenz einer moderaten bis schweren COVID-19-Erkrankung betrug ≥14 Tage nach Impfung 164,8 / 1000 Personenjahre in der Placebo- und 55,6 / 1000 Personenjahre in der Ad26.COV2.S-Gruppe. Schwere bis kritische Erkrankungen traten mit einer Inzidenz von 25,6 bzw. 6,1 / 1000 Personenjahre auf. Nach ≥28 Tagen betrugen diese Inzidenzwerte 25,6 und 6,1 bzw. 15,6 und 2,6 / 1000 Personenjahre. Die Vakzin-Effektivität (Abbildung 1) ist mit derjenigen des AstraZeneca-Impfstoffs vergleichbar und zeigt insbesondere keine wesentlichen Unterschiede gegen die südafrikanischen und brasilianischen Virus-Varianten.
Bei jedem 44. Geimpften < 60 und jedem 91. ≥ 60 Jahren der Vakzin-Gruppe wurden systemische unerwünschte Arzneimittelreaktionen beobachtet. Die Rate schwerer (Grad 3 und höher) unerwünschter Ereignisse betrug sowohl in der Impfstoff- als auch der Placebo-Gruppe jedoch nur 0,1 % (The New England Journal of Medicine).
In der Vakzin-Gruppe (n=21895) wurden 6 (0,027 %) tiefe Beinvenenthrombosen, 4 (0,018 %) Lungenembolien und eine Sinus-Thrombose (0,005 %) beobachtet. In der Placebo-Gruppe (n=21888) traten diese Ereignisse in 4, 1 und 0 Fällen auf.
Fazit
Die Vakzine Ad26.COV2.S des Herstellers Janssen-Cilag / Johnson & Johnson kann das Impfspektrum gegen COVID-19 erheblich erweitern. Ähnlich wie beim Vektorimpfstoff Vaxzevria von AstraZeneca wurde im Rote-Hand-Brief auf das seltene Auftreten eines VIPIT / VITT Syndroms hingewiesen, welches auf Bevölkerungsebene einer zusätzlichen behördlichen Überwachung bedarf.
Stand: 29.04.2021
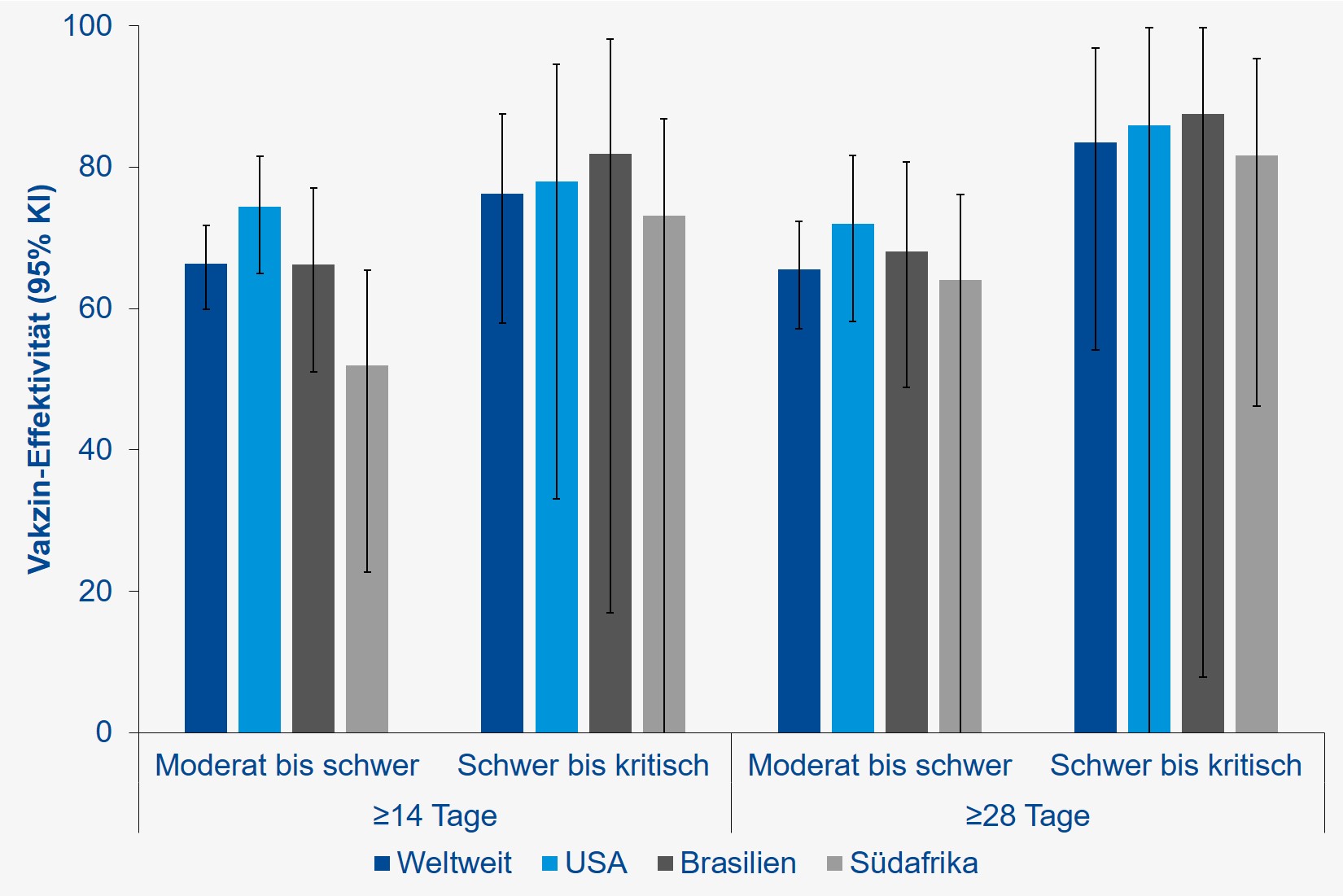
Abb. 1
Effektivität der Vakzine Ad26.COV2.S im Vergleich zu Placebo ≥14 und ≥28 Tage nach Impfung. Stratifizierung gemäß COVID-19-Schweregrad und Studienregion. Grafische Darstellung nach (The New England Journal of Medicine)