Antikörperkonzentration in Spenderplasma
Eine US-amerikanische Registeranalyse untersuchte den Einfluss verschiedener Antikörperkonzentrationen im Spenderplasma auf den Verlauf einer COVID-19-Erkrankung.
Im April 2020 wurde durch die US-amerikanische Food and Drug Administration (FDA) und die Mayo-Clinic das COVID-19 Convalescent Plasma Expanded Access Program (EMA) initiiert, um den Zugang zu Konvaleszenten-Plasma als Therapieoption bei COVID-19 zu erleichtern und dessen Wirksamkeit und Sicherheit zu überprüfen. Nach Einschluss von über 100.000 Patientinnen und Patienten an 2.780 Kliniken in den USA erteilte die FDA im August 2020 eine Notfallzulassung für den therapeutischen Einsatz von Spenderplasma.
In einer Stichprobe der EMA-Datenbank wurde der Einfluss der Konzentration von IgG-Antikörpern in transfundierten Proben auf den Erkrankungsverlauf untersucht (The New England Journal of Medicine). Der IgG-Gehalt wurde mittels einer Farbreaktion (Chemilumineszenz) bei Bindung des Antikörpers an eine Untereinheit des SARS-CoV-2-Spike-Proteins gemessen und als dimensionsloser Signalkoeffizient („signal-to-cutoff-ratio“) angegeben. Letzterer wurde als niedrig (<4,6), mittel (4,6 bis 18,5) oder hoch (>18,5) klassifiziert.
Ausgewertet wurden Daten von 3.082 Behandelten aus 680 Kliniken landesweit. Hiervon waren 57 % über 60 Jahre alt, 61 % Männer, 53 % fettleibig, 48 % Kaukasier. Eine schwere oder lebensbedrohliche COVID-19-Erkrankung lag in 65 % aller Fälle vor, 33 % wurden vor der Plasma-Infusion mechanisch beatmet. Die pharmakologische Therapie umfasste u.a. Remdesivir (31 %) und Corticosteroide (51 %), aber auch mittlerweile durch Studiendaten entkräftete Substanzen wie Azithromycin (54 %) und Hydroxychloroquin (33 %).
Die untersuchte Gruppe umfasste 561, 2.006 und 515 Patientinnen und Patienten, welche Plasmaspenden mit niedrigen, mittleren und hohen Antikörpertitern erhielten. Die 30-Tage-Sterblichkeit nahm dosisabhängig ab (Abb. 1). Dieser Effekt wurde aber praktisch ausschließlich bei Nicht-Beatmeten beobachtet (Tabelle 1). Auch der Transfusionszeitpunkt war entscheidend: Wurde Konvaleszenten-Plasma innerhalb von drei Tagen nach der COVID-19-Diagnose infundiert, betrug die 30-Tage-Sterblichkeit 22 % (95 % Konfidenzintervall [KI] 20 – 25 %), bei späterer Gabe 30 % (95 % KI 28 – 32 %).
Fazit
Daten des US-amerikanischen EMA-Registers legen nahe, dass im Falle der Entscheidung zur Therapie mit Konvaleszenten-Plasma dieses früh (innerhalb von drei Tagen nach COVID-19-Diagnose) bei Nicht-Beatmeten gegeben werden sollte und hohe Titer von Anti-SARS-CoV-2-Antikörpern aufweisen muss, um den Erkrankungsverlauf günstig zu beeinflussen.
Stand: 22.01.2021
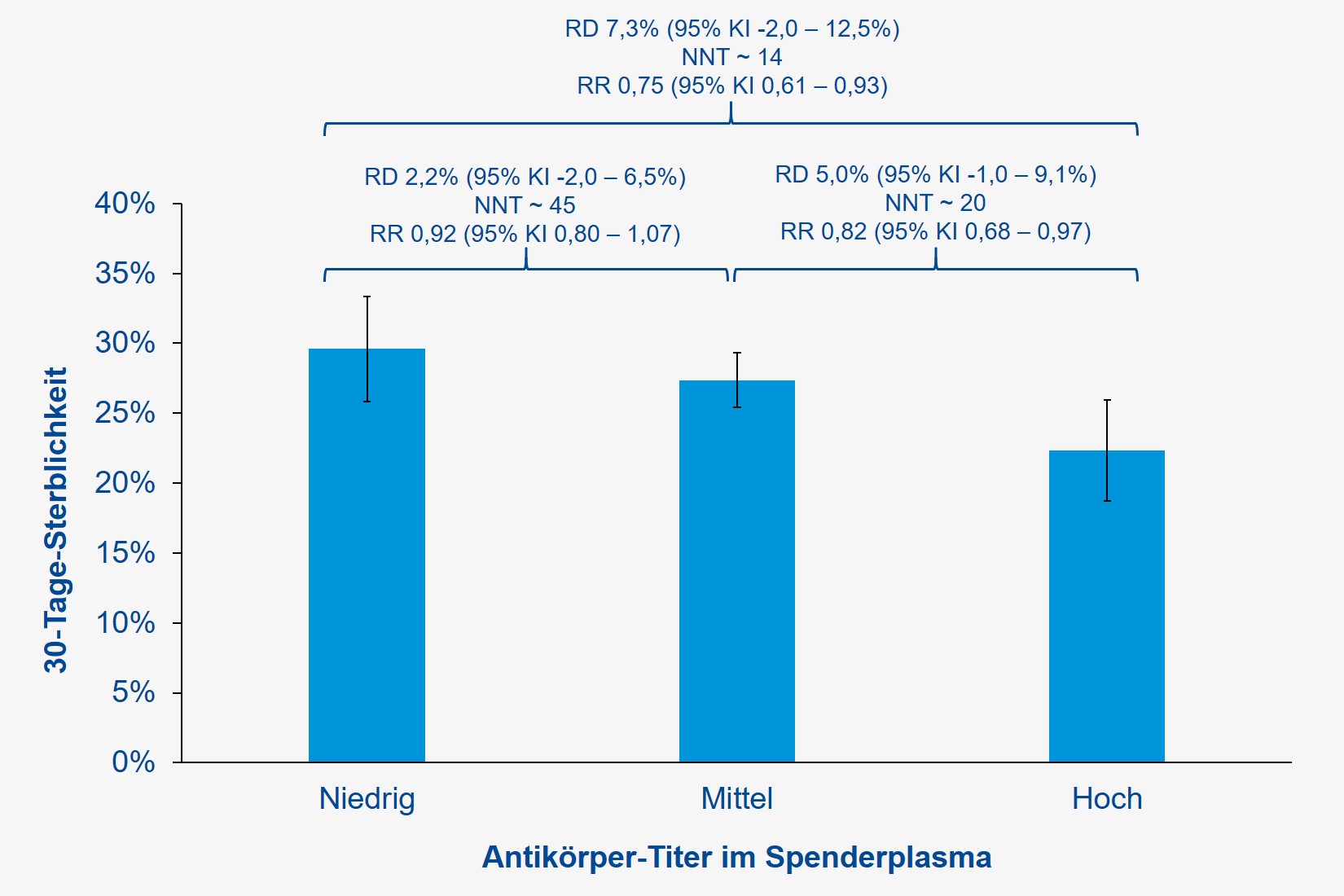
Abb.
30-Tage-Sterblichkeit in Abhängigkeit vom Antikörpertiter gegen SARS-CoV-2 in therapeutisch verabreichtem Spenderplasma. Nachberechnet nach The New England Journal of Medicine.
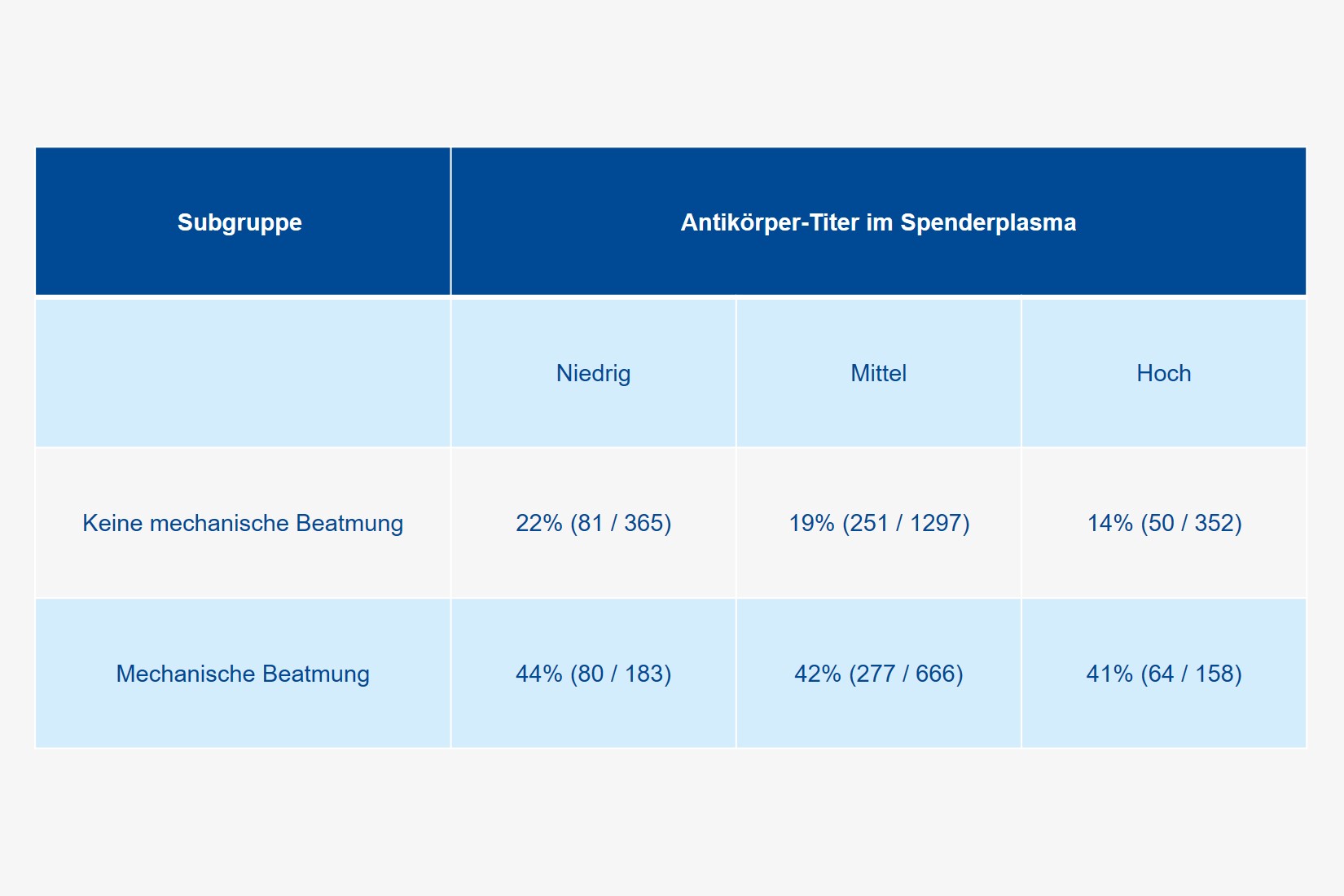
Tab.
30-Tage-Sterblichkeit in Abhängigkeit vom Antikörpertiter gegen SARS-CoV-2 in therapeutisch verabreichtem Spenderplasma und einer mechanischen Beatmung. Nach The New England Journal of Medicine.